どうもこんにちは、Megです。
以下の論文のサーベイメモをまとめていきます。

内容における解釈違いの可能性があることをご容赦ください…!
サーベイ論文
X. Liu et al., “Decoding ECoG High Gamma Power from Cellular Calcium Response using Transparent Graphene Microelectrodes,” 2019 9th International IEEE/EMBS Conference on Neural Engineering (NER), 2019, pp. 710-713, doi: 10.1109/NER.2019.8717147.

研究の概要
ECoG(Electrocorticography):ヒトの脳研究で広く使用されている脳波の一種。
二光子顕微鏡:動物モデルにおける神経科学研究に適用。
→ECoGと二光子顕微鏡のギャップを埋めることで、動物モデルの神経科学の知見を、ヒトの脳研究に適用可能。
ECoG記録と透明グラフェン微小電極アレイを使用し、カルシウムイメージングによる細胞カルシウム活動から、high-γをデコードするLSTMを開発。
覚醒・麻酔状態の両方で、ECoGのhigh-γを正常にデコードできた。
問題設定と解決した点
動物実験で得られた知見をヒトの脳研究に転用するためには、ECoGと二光子顕微鏡の方法論のギャップを埋める必要がある。
→細胞のカルシウム活動から、観測されたECoG電位を解読できるモデルを構築することが重要。
本研究では、
- 透明グラフェン微小電極アレイを用いて、電気生理(ECoG)記録と二光子カルシウムイメージングを行い、同時にECoG信号と細胞活動の関係を明らかにする。
- 同時に記録されたECoG信号と、個々のニューロンからのカルシウム蛍光応答を用いて、リカレントニューラルネットワーク(LSTM)モデルを学習し、ECoG信号をデコードする。
を目的とした。
技術や手法のキモ
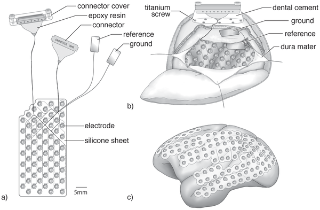
透明グラフェン微小電極アレイ
透明グラフェン微小電極アレイを用いることで、20日間以上安定したインピーダンスを保つことができた。
透明な電極アレイを使用することで、脳波信号の記録と同時に、カルシウムイメージングを実施することができた。
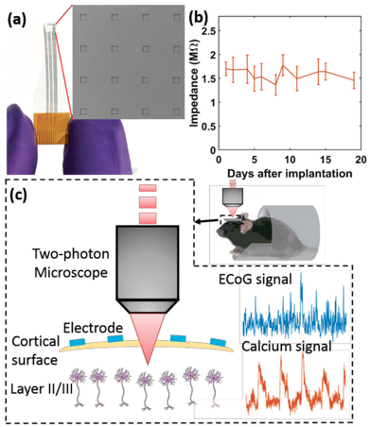
から引用
LSTM
LSTMを使用することで、カルシウムイメージングで記録した細胞スパイク活動からECoGを予測しデコードした。時間tにおけるECoGのhigh-γパワーを予測するために、前の9つの時間ステップからの細胞スパイク活動を考慮するモデルを実装した。
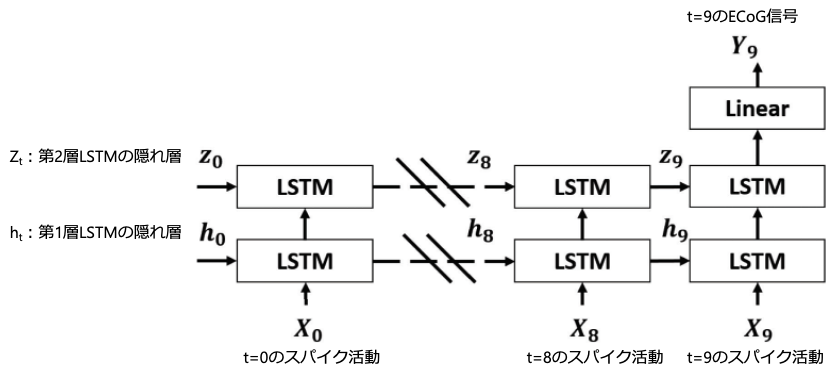
から引用、改変
有効性の検証
カルシウムイメージング
覚醒状態:ROIにおける細胞蛍光の上昇による、安定した刺激誘発性視覚応答があった。スパイク活動も上昇したが、まばらで確率的。
麻酔状態:細胞蛍光シグナルは、麻酔中によく観察されニューロン発火を調整する振動に起因する、1~2Hzのゆらぎを示した。
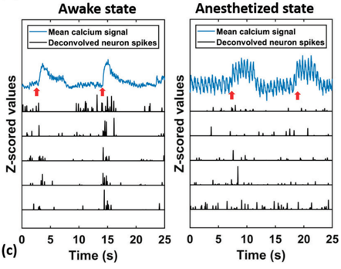
から引用
LSTMによるECoGデコード
麻酔状態では、正常にECoGをデコードできた。視覚刺激がない状態では、1~2Hzのゆらぎも再現できた。
覚醒状態でも、刺激オン・オフ反応をデコードできた。しかし、視覚刺激がない状態では、信号はあまり同期していない。
覚醒状態・麻酔状態ともに、どちらも高い相関を示した。だが、覚醒状態の分散が若干大きいのは、覚醒状態では神経細胞が活性化し、非同期化するためである。
→開発モデルは、麻酔・覚醒状態ともに第Ⅱ/Ⅲ層のニューロンからの細胞活動を用いて、ECoGのhigh-γパワーを低分散でデコードした。
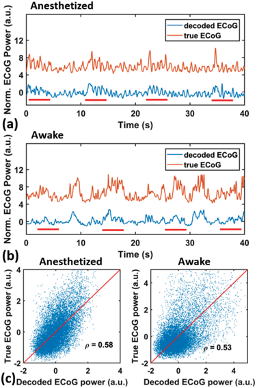
から引用
議論
- ECoG信号と2光子カルシウムイメージングの両方で、20日間にわたる安定した慢性記録を実現した。
- 開発したLSTMリカレントニューラルネットワークは、覚醒状態と麻酔状態の両方において、刺激中および無刺激時のECoGのhigh-γパワーのデコードに成功した。
- 本研究は、電気生理学によって得られたヒトの臨床研究の知見を、動物モデルの高解像度二光子顕微鏡によって得られた発見と結びつける研究であるといえる。
次に読むべき論文
ECoGとhigh-γについて勉強したい。
S. Ray and J. H. Maunsell, “Different origins of gamma rhythm and high-gamma activity in macaque visual cortex,” PLoS Biol, vol. 9, no. 4, p. e1000610, Apr 2011.
G. Buzsaki and X. J. Wang, “Mechanisms of gamma oscillations,” Annu Rev Neurosci, vol. 35, pp. 203-25, 2012.