どうもこんにちは,Megです.
以下の論文のサーベイメモをまとめていきます.
フォーマットは「Chem-Station,”研究者目線からの論文読解を促す抄録フォーマット”,2017.」を参考にさせていただきました.
論文内容における解釈違いの可能性があることをご容赦ください…!
サーベイ論文
Akeju, Oluwaseun, Song, Andrew H., Hamilos, Allison E., Pavone, Kara J., Flores, Francisco J., Brown, Emery N., Purdon, Patrick L. Electroencephalogram signatures of ketamine anesthesia-induced unconsciousness. Clinical Neurophysiology. 2016, vol. 127, no. 6, p. 2414–2422.
研究の概要
ケタミンは,全身麻酔として投与されるN-メチル-D-アスパラギン酸(N-methyl-D-aspartate:NMDA)受容体拮抗薬である.
人間のケタミン誘発性の無意識を説明する神経回路レベルのメカニズムはまだ定義されていない.よって,ケタミン誘発性の意識喪失において脳波(electroencephalogram:EEG)マーカーが存在するかを調べた.
方法として,ケタミンを投与された12人の患者のEEGを,パワースペクトルとコヒーレンス法を使用して分析した.
結果は,ケタミンを投与して意識喪失を誘発した後,低速δ(0.1~4Hz)とγ振動(〜27~40Hz)を交互に繰り返す「ガンマバースト」を観察した.このEEGパターンは,θ振動(〜4~8Hz)の増加とα/β振動(〜10~24Hz)の減少にも関連していた.
これらから,ケタミンによる意識消失は,ガンマバーストEEGパターンと関連していることが示された.
問題設定と解決した点
ケタミンは全身麻酔に利用できる数少ない麻酔薬である.
しかし,ケタミン誘発性の意識喪失中の脳を監視するために利用できる神経生理学的な刺激が欠けているため,これを説明する神経回路レベルのメカニズムはまだ理解されていない.
技術や手法のキモ
データセット
マサチューセッツ総合病院で12人の被験者に対して,全身麻酔とEEG採集を行った.
Table 1に患者の特徴と併用薬を示す.
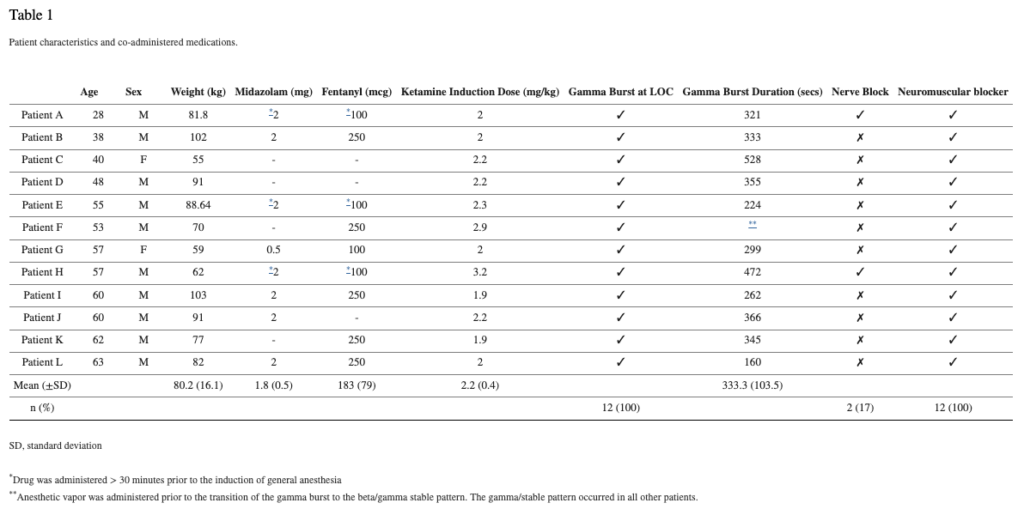
コヒーレンス分析
2つの信号$x, y$の間のコヒーレンス$C_{xy}(f)$(1)は次のように定義される.
$$C_{xy}(f) = \frac{|S_{xy}(f)|}{\sqrt{S_{xx}(f)S_{yy}(f)}}$$
ここで,
$|S_{xy}(f)|$:$x(t), y(t)$間のクロススペクトル
$(f)$:信号$x(t)$のパワースペクトル
$S_{yy}(f)$:信号$y(t)$のパワースペクトル
である.
コヒーレンスは,周波数依存の相関係数として解釈したり,同じ周波数の2つの信号感の関連付けの尺度として解釈することもできる.
有効性の検証
スペクトル分析
ベースラインとケタミン誘発EEGの代表的なスペクトログラムと時間領域での脳波変化をFigure 1に示した.
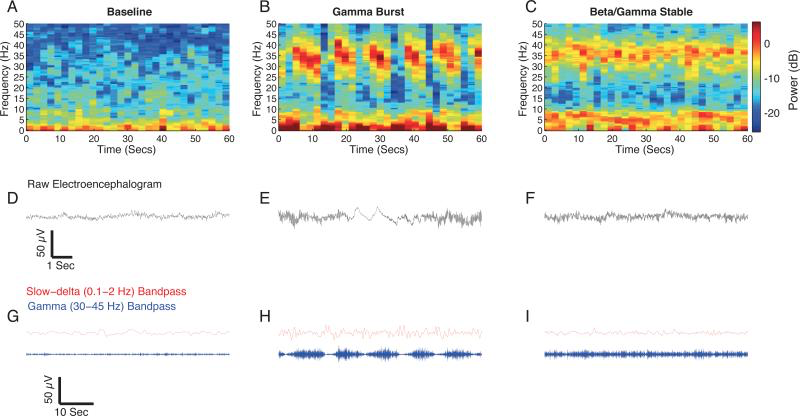
Figure 1A, B, C:ベースライン・ガンマバースト・β/γ stableのスペクトログラム
Figure 1D, E, F:ベースライン・ガンマバースト・β/γ stableのスペクトログラムに対応する脳波
Figure 1G, H, I:スローδバンドパスとγバンドパスを通過したEEG
を示している.
Figure 1Bから,スローδ・θ・γ周波数帯域にパワーが集中しており,増加したγパワーとδ振動は交互に規則的なパターンで発生したことが観測できた.Figure 1EはFigure 1Bの生のEEGであり,これからも交互のδ振動とγ振動は見て取れる.
Figure 1C, Fはβ/γ stableスペクトログラムとそれに対応するEEGである.ガンマバーストと比較すると,これらのγパターンは規則的ではない.
Figure 4は,ベースライン・ガンマバースト・β/γ stableをグループレベルで比較するスペクトル分析である.
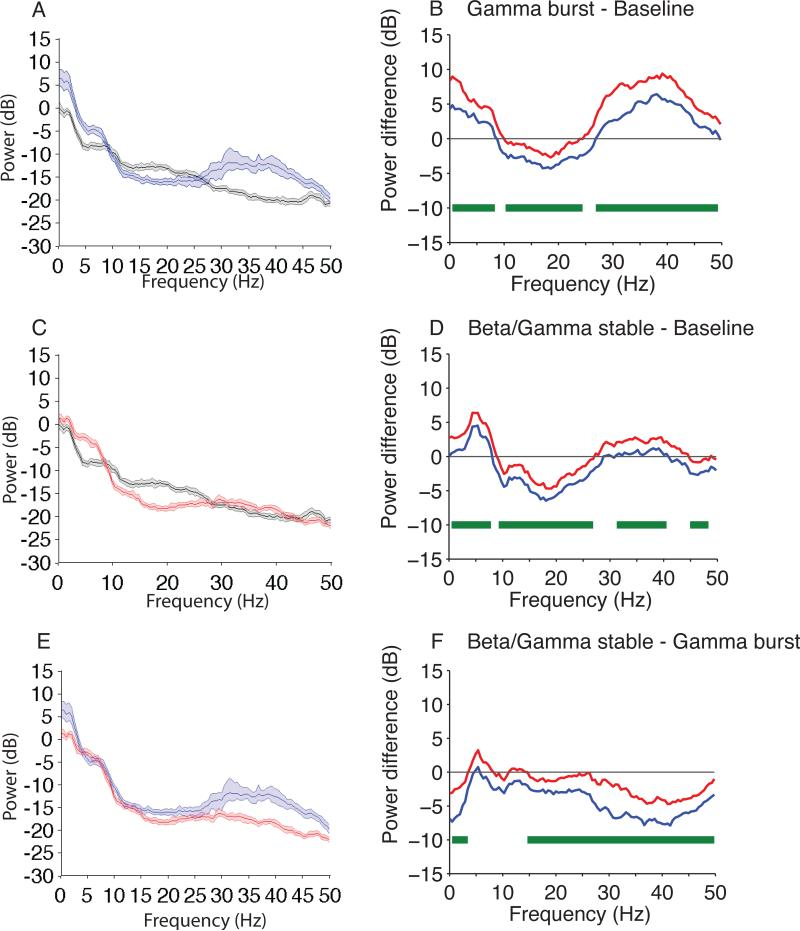
Figure4A, C, E:ベースライン(黒)・ガンマバースト(青)・β/γ stable(赤)において,2グループ間のパワースペクトル.影付きの領域は95%信頼区間を示す.
Figure4B, D, F:左図でのスペクトル間の差の95%信頼区間の境界を表す.
Figure 4Aから,ガンマバーストのEEGパワーは,0.1~8.3Hz・26.9~50Hzでベースラインよりも大幅に大きく,10.3~24.4Hzでベースラインよりも小さい.
Figure 4Cから,β/γ stableのEEGパワーは,0.1~7.8Hz・31.25~40Hzでベースラインよりも大幅に大きく,9.2~26.9Hz・44.9~48.3Hzでベースラインよりも小さい.
Figure 4Eから,ガンマバーストのEEGパワーは,0.1~3.4Hz・16.1~50Hzでβ/γ stableよりも有意に大きい.
コヒーレンス分析
Figure 5は0~50Hzの周波数範囲内のグループレベルのコヘログラムである.
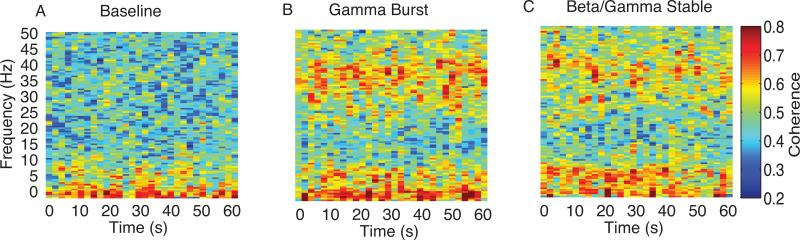
Figure 5Bから,ガンマバーストはベースラインと比較して,低速のδ・θ・γ周波数帯域でコヒーレンスが増加していた.
Figure 5Cから,β/γ stableはベースラインと比較して,θ・γ周波数帯域でパワーが増加し,α/β周波数帯域でパワーが減少していた.
Figure 6は,ベースライン・ガンマバースト・β/γ stableをグループレベルで比較するコヒーレンス分析である.
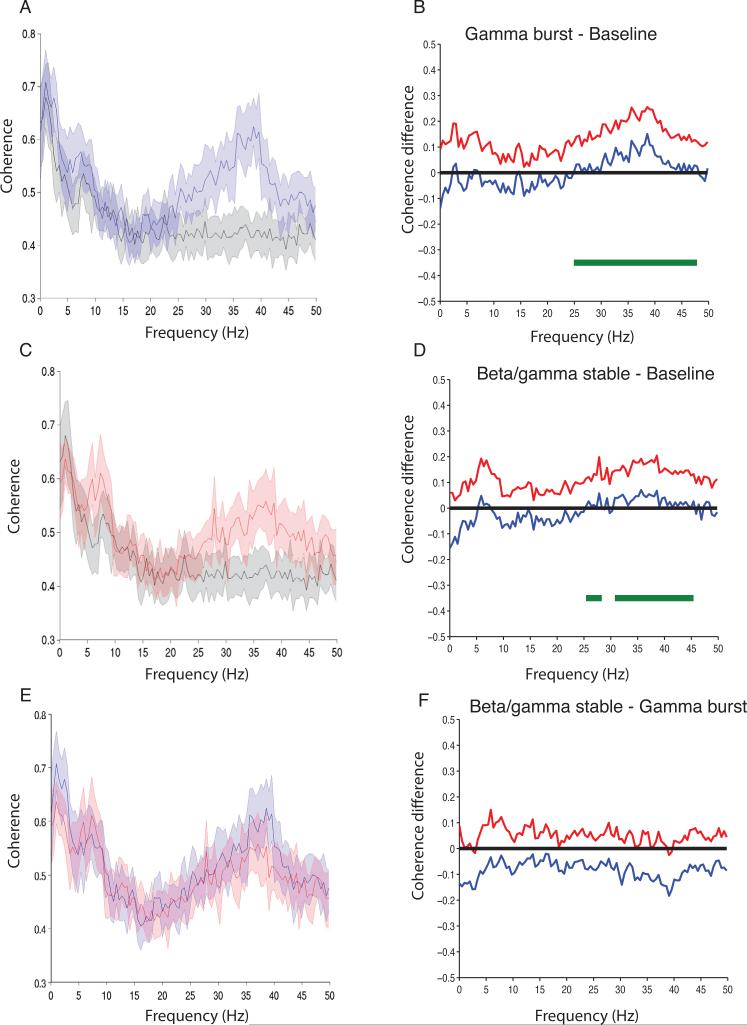
Figure6A, C, E:ベースライン(黒)・ガンマバースト(青)・β/γ stable(赤)において,2グループ間のコヒーレンス解析.影付きの領域は95%信頼区間を示す.
Figure6B, D, F:左図でのコヒーレンス間の差の95%信頼区間の境界を表す.
Figure4B, D, F:左図でのスペクトル間の差の95%信頼区間の境界を表す.
Figure 6Aから,ガンマバーストのEEGは,27.9~48.9Hzでベースラインよりも有意にコヒーレントだった.
Figure 6Cから,β/γ stableのEEGパワーは,25.4~28.3Hz・30.8~45.5Hzでベースラインよりも有意にコヒーレントだった.
Figure 6Eから,EEGコヒーレンスはガンマバースト・β/γ stableの両方で同様だった.
議論・結論
- 全身麻酔レベルのケタミンでは,γ振動 (ガンマバースト) と交互になるスロー δ振動が発生する.
- γ・θ・α/β振動の減少は、全身麻酔レベルでのケタミンに固有のものではない.
- ガンマバーストパターンは、皮質および皮質下部位での回路の混乱に起因する可能性がある.
次に読むべき論文
ケタミンは統合失調症の研究モデルとしても使われている.
Insel, Thomas R. Rethinking schizophrenia. Nature. 2010, vol. 468, no. 7321, p. 187–193.
参考文献
(1)“fMRI解析の基礎 (9):コヒーレンス解析”.

付録
この研究では,スペクトル分析とコヒーレンス分析にMATLABのChronuxツールボックスを使用している.